[식약처]메디톡신주 등에 대한 회수·폐기 및 잠정 제조·판매·사용 중지(의약품 안전성 속보)
첨부파일
-
- 첨부파일: 별첨.식약처 의약품 안전성 속보.pdf (140.5K)182
-
- 첨부파일: 식약처.jpg (20.0K)228
짧은주소
본문
[식약처]메디톡신주 등에 대한 회수·폐기 및 잠정 제조·판매·사용 중지(의약품 안전성 속보)
- 국가출하승인 받지 않고 판매한 메디톡신주 등 회수·폐기 명령 등 조치
- 품목허가 취소 등 행정처분 절차 착수 및 잠정 제조·판매·사용 중지
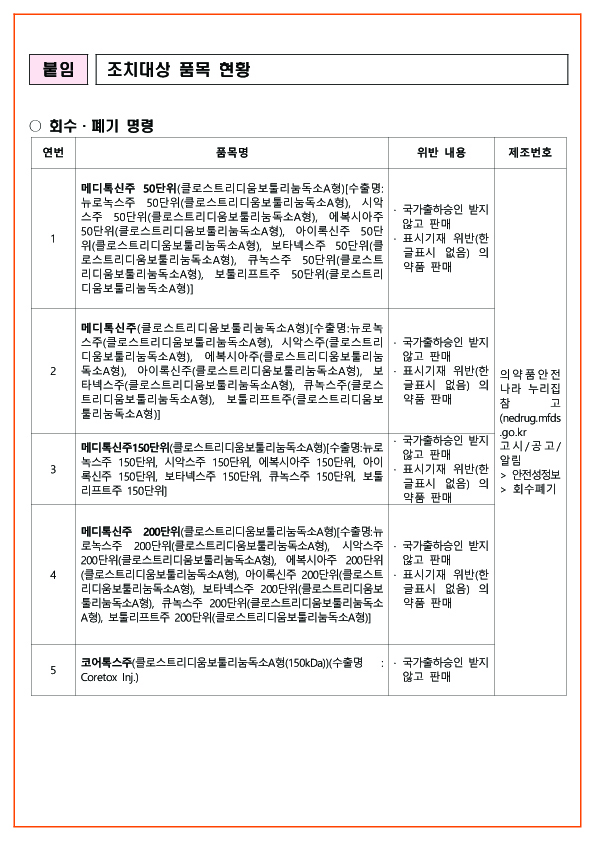
- 회수·폐기 대상: 메디톡신주(50・100・150・200단위) 및 코어톡스주 제품 중 국가출하승인을 받지 않았거나 한글표시가 없는 제조단위
식품의약품안전처(처장 이의경)는 ㈜메디톡스社가 메디톡신주 등을 국가출하승인 받지 않고 판매한 사실 등을 확인하여 ’20.10.19.자로 해당 제품에 대하여 회수·폐기 명령하고, 품목허가 취소 등 행정처분 절차에 착수합니다.
식약처는 ㈜메디톡스社가 국가출하승인 대상 의약품인 보툴리눔 제제를 국가출하승인을 받지 않거나 표시기재 규정을 위반(한글표시 없음)하여 판매하는 등 약사법 위반사항을 확인하였습니다.
국가출하승인을 받지 않고 판매한 제품은 메디톡신주 50・100・150・200단위 및 코어톡스주의 일부 제조단위이며, 한글표시 없이 판매한 제품은 메디톡신주 50・100・150・200단위의 일부 제조단위입니다.
식약처는 국가출하승인을 받지 않거나 표시기재 규정을 위반한 메디톡신주 50・100・150・200단위, 코어톡스주의 해당 제조단위에 대하여 회수·폐기를 명령했습니다.
* 회수·폐기 대상: 메디톡신주(50・100・150・200단위) 및 코어톡스주 제품 중 국가출하승인을 받지 않았거나 한글표시가 없는 제조단위
식약처는 국가출하승인 대상인 보툴리눔 제제를 국가출하승인 받지 않고 판매한 행위에 대해서는 약사법 제53조 제1항 위반으로 품목 허가취소 행정처분 절차에 착수하였습니다.
* 품목허가 취소 예정 품목: 메디톡신주 50・100・150・200단위, 코어톡스주
아울러, 의약품을 판매할 수 없는 자에게 의약품을 판매한 행위 및 한글표시가 없는 의약품을 판매한 행위에 대해서도 약사법 제47조 제1항 제1호 및 제61조 제1항 위반으로 판매업무 정지 등 행정처분 조치할 예정입니다.
* 행정처분 예정 품목: 메디톡신주 50・100・150・200단위, 이노톡스주, 코어톡스주
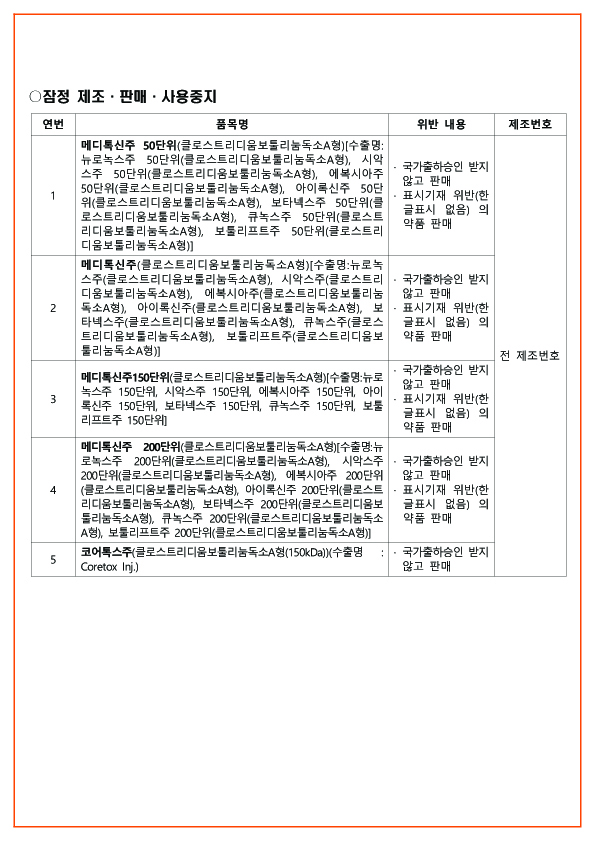
식약처는 허가취소 대상 품목에 대해 행정절차상 소요되는 기간을 고려하여 소비자 보호 및 사전 예방 차원에서 잠정적으로 제조·판매 중지를 명령하는 한편, 의료인과 건강보험심사평가원 및 관련 단체에 즉각적인 사용 중지를 요청하며 안전성 속보를 배포하였습니다.
또한, 식약처는 해당 의약품 제조업체에 대한 행정절차를 신속히 진행할 예정이며, 의료인 및 관련 단체에 업체의 회수·폐기 절차에 적극 협조하여 줄 것을 당부했습니다.
▶별첨: 식약처 의약품 안전성 속보






























댓글목록
등록된 댓글이 없습니다.