로슈, 여드름 치료제 '로아큐탄' 공급 중단
18,391
2019.02.15 16:16
첨부파일
-
- 첨부파일: 로아큐턴.jpg (24.3K)981
짧은주소
본문
로슈, 여드름 치료제 '로아큐탄' 공급 중단
- 구체적 안내 없이 도매·약국에 공문
- 대체 품목은 다수 유통
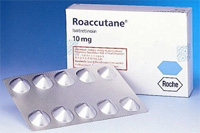
한국로슈가 여드름치료제 '로아큐탄 캡슐' 공급을 중단했다.
한국로슈는 최근 각 유통업체에 '로아큐탄 캡슐 공급 중단' 공문을 통해 구체적인 시기와 방법은 논의 중에 있다고 밝혔다.
회사는 "로아큐탄 캡슐 판매가 중단된다"며 "세부 일정은 논의 중으로 빠른 시일 내에 다시 공지하겠다"고 설명했다.
공문에는 판매 중단을 결정한 이유, 공급 중단 시기 등 구체적인 내용은 없었다.
유통업체와 약국 역시 공급 중단 사실과 원인에 대해 아는 곳이 없었다. 다만, 특허 만료 이후 50가지 이상의 제네릭이 쏟아져 나왔고, 이로 인해 처방량이 현저히 줄어들어 본사가 로아큐탄의 한국 시장 공급을 포기한 것 아니냐는 추측이 나오고 있다.
로아큐탄은 이전에도 품절돼 약국에 불편을 유발한 바 있다. 2000년대 후반에는 독감이 유행해 로슈가 공장 라인을 모두 '타미플루' 생산에 집중하며 잠시 공급이 중단된 바 있다. 또 단순 수급불균형으로 종종 품절됐었다.
이소트레티노인 제제인 로아큐탄은 일반인에게도 잘 알려진 중증 여드름 치료제다. 그러나 기형아 유발성이 매우 높아 임신 가능성이 있는 여성에게 금기 약물이다. 최근에는 발기부전이 이상반응으로 추가됐다.
최근에는 제네릭 처방이 많지, 오리지널 처방은 많이 줄어들었다고 한다.






























댓글목록
대피연님의 댓글
▷이소트레티노인 품목 취하 러시, 부작용 논란에 매출 하락
- 8개 품목 허가 자진 취하…제약사 "매출 하락에 부작용 이슈로 품목 유지 요인 적어"
부작용 이슈에 시달린 비타민 A 유도체의 매출 저하가 본격화되면서 자진 품목 취하 움직임이 나타나고 있다.
일부 품목의 경우 매출액이 연간 1천만원 대에 그치는 등 실익이 크지 않은 만큼 태아 기형 유발 가능성 문제로 시판 후 의약품의 위해성 관리계획(RMP)제출 대신 품목 취하를 선택한 것으로 풀이된다.
24일 제약업계에 따르면 내달 동광제약 뉴티논연질캡슐, 대한뉴팜 아크논연질캡슐 등 이소트레티노인 성분 8품목이 약제 급여 목록에서 및 급여 상한금액표에서 삭제된다.
이소트레티노인 성분은 비타민 A 유도체로서 여드름 치료제로 사용된다. 이소트레티노인은 중증의 여드름 치료제로 태아에게 심각한 기형을 유발할 가능성이 높아 임부에게는 사용을 금지하며 임신 가능성이 있는 여성 또한 주의해야 한다.
해당 부작용은 흔히 알려져 있었지만 올해 초 국회에서 부작용에 따른 이소트레인 관리 프로그램 도입 간담회를 개최하면서 부작용 이슈가 부각됐다.
식품의약품안전처에 이어 의약품안전관리원도 이소트레티노인 성분 품목에 대한 안전 사용과 주의를 촉구하면서 이소트레티노인 성분 뿐 아니라 타 적응증에 사용되는 알리트레티노인, 아시트레틴도 매출 하락이 가시화됐다.
복지부 관계자는 "해당 품목의 상한금액 삭제는 복지부가 미생산이나 보험급여 내역이 없는 품목을 조사, 자체적으로 삭제한 게 아니"라며 "제약사가 직접 식약처에 품목 취하를 요청한 내역을 토대로 급여 삭제된 것이다"고 밝혔다.
이소트레티노인 성분 품목은 동아에스티, 동구바이오 등 24개 제약사가 품목을 생산, 유통하고 있다. 8개 품목은 전체의 1/3에 해당하는 수치.
품목을 자진 취하한 제약사 관계자는 "최근 해당 품목의 허가를 자진 취소했다"며 "매출액도 낮은데 부작용 이슈까지 겹치면서 굳이 품목을 유지할 이유가 없어졌다"고 설명했다.
실제로 취하 품목의 최소 매출액은 연간 1000만원에서 최대 3억 7300만원에 불과하다.
의약품 시장 조사 기관 유비스트에 따르면 작년 2분기 대비 올해 2분기 비타민 A 유도체 13개 품목 매출은 평균 8.6% 하락했다.
이소트레티노인은 오리지널 로아큐탄과 마더스제약 로이탄, 동구바이오 트레논만 각각 16.6%, 24.7%, 0.1% 상승했을 뿐 나머지 8개 품목은 평균 17.1% 하락했다.
특히 고려제약 이소트렌과 코오롱 트레틴, 동아에스티 아크날의 하락폭이 평균 33.7%로 컸다.
식약처는 위 품목의 태아 기형 유발 가능성을 이유로 동 성분을 함유한 허가(신고)의약품을 보유한 업체에 대해 이달까지 위해성 관리계획을 의약품안전평가과에 제출하도록 지시했다.